Aparentemente esta bien presentado el efecto debe ser a largo plazo
Sehr gut verträglich. Ich verspürte eine Verbesserung nach wenigen Tagen.
Nicotinamid-Mononukleotid — kurz NMN — ist ein Vitamin-B3-Derivat und die direkte biochemische Vorstufe von NAD⁺, einem Coenzym, das in jeder menschlichen Zelle an der Energieproduktion, DNA-Reparatur und Regulation zentraler Stoffwechselprozesse beteiligt ist. Mit zunehmendem Alter sinkt der zelluläre NAD⁺-Spiegel messbar — NMN wird in der Longevity-Forschung als möglicher Ansatz untersucht, diesen Rückgang auszugleichen.
Diese Seite fasst den biochemischen Mechanismus, den aktuellen Forschungsstand und den regulatorischen Status von NMN in der EU zusammen — sachlich eingeordnet, wissenschaftlich differenziert und auf das Wesentliche konzentriert.
NMN — chemisch β-Nicotinamid-Mononukleotid — ist ein Nukleotid, das natürlicherweise in menschlichen Zellen vorkommt und als unmittelbare Vorstufe von NAD⁺ (Nicotinamid-Adenin-Dinukleotid) eine zentrale Rolle im Energiestoffwechsel einnimmt. Strukturell gehört NMN zur Familie der Vitamin-B3-Derivate: Es besteht aus einem Nicotinamid-Ring, einer Ribose-Einheit und einer Phosphatgruppe.
In der Nahrung kommt NMN in Spuren vor — unter anderem in Edamame, Brokkoli, Avocado und einigen Fleischsorten. Die über die Ernährung aufgenommenen Mengen sind jedoch biochemisch gering; sie liegen deutlich unterhalb der Mengen, die in Forschungsstudien eingesetzt werden.
In der Longevity-Forschung werden mehrere NAD⁺-Vorstufen untersucht. Die drei am häufigsten diskutierten sind NMN, NR (Nicotinamid-Ribosid) und die direkte Zufuhr von NAD⁺.
NMN und NR unterscheiden sich strukturell durch eine zusätzliche Phosphatgruppe bei NMN. Beide werden intrazellulär in NAD⁺ umgewandelt, über leicht unterschiedliche Synthesewege: NR wird zunächst in NMN umgewandelt, bevor es als NAD⁺ verfügbar ist. NMN tritt diesen Schritt direkt an.
Die direkte Supplementierung von NAD⁺ wird durch die Molekülgröße limitiert: NAD⁺ kann zelluläre Membranen nicht ohne weiteres passieren. Kleinere Vorstufen wie NMN gelangen leichter in die Zelle und werden dort erst in NAD⁺ überführt. Dieser Aufnahmemechanismus ist Gegenstand laufender Forschung — unter anderem wurde 2019 ein spezifischer NMN-Transporter (Slc12a8) in Mäuse-Darmzellen beschrieben (Grozio et al., Nature Metabolism, 2019).
NAD⁺ wird im Körper kontinuierlich synthetisiert und verbraucht. Mit zunehmendem Alter verschiebt sich dieses Gleichgewicht: Die Syntheserate nimmt ab, während der Verbrauch durch DNA-Reparaturprozesse und Entzündungsreaktionen steigt. Studien zeigen, dass der zelluläre NAD⁺-Spiegel beim Menschen ab dem mittleren Lebensalter messbar sinkt — in einigen Geweben auf bis zu 50 % des Ausgangswertes (Zhu et al., PNAS, 2015). Dieser Rückgang wird mit verminderter mitochondrialer Funktion, verlangsamter Zellregeneration und veränderten epigenetischen Regulationsprozessen in Verbindung gebracht.
NMN wird in diesem Kontext als Substrat untersucht, das den körpereigenen NAD⁺-Syntheseweg — den sogenannten Salvage-Pathway — gezielt speisen kann.
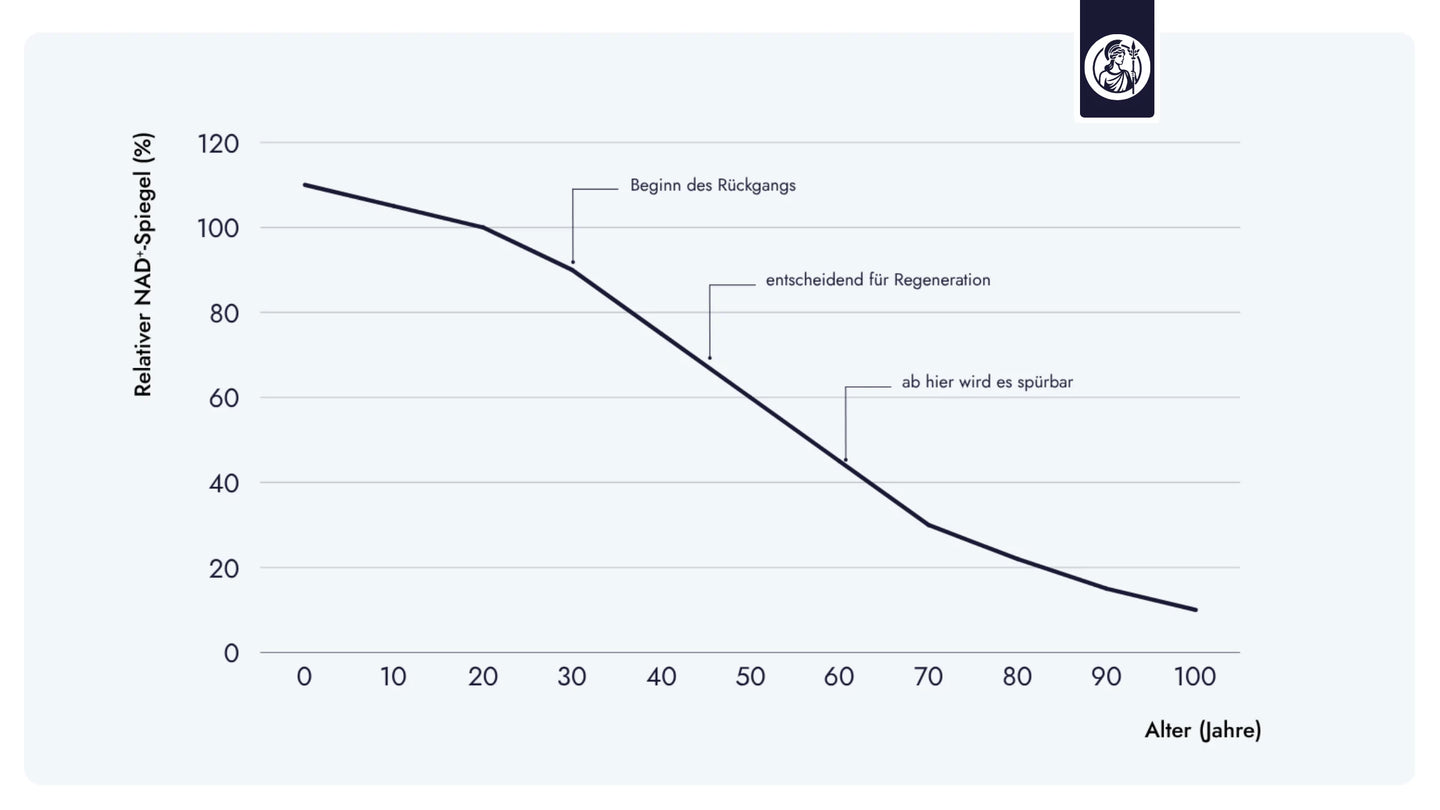
Schematische Darstellung basierend auf wissenschaftlichen Beobachtungen zum altersbedingten Rückgang von NAD+.
NAD⁺ ist kein Nährstoff im klassischen Sinne — es ist ein Coenzym, das in jeder menschlichen Zelle an über 500 enzymatischen Reaktionen beteiligt ist. Ohne NAD⁺ kommt die mitochondriale Energieproduktion zum Stillstand; DNA-Reparaturprozesse können nicht ablaufen; epigenetische Regulationsmechanismen verlieren ihre Grundlage.
NMN gelangt in die Zelle und wird dort in einem einzigen enzymatischen Schritt durch das Enzym NMNAT (Nicotinamid-Mononukleotid-Adenylyltransferase) direkt in NAD⁺ umgewandelt. Dieser Weg ist Teil des sogenannten Salvage-Pathways — dem wichtigsten Recycling-Mechanismus für NAD⁺ im menschlichen Körper.
Eine der zentralen Enzymfamilien, die NAD⁺ als Substrat benötigen, sind die Sirtuine (SIRT1–SIRT7). Sie regulieren unter anderem die Genexpression, mitochondriale Biogenese, Entzündungsreaktionen und DNA-Reparaturprozesse. Sirtuine verbrauchen NAD⁺ bei jeder Reaktion — sinkt der NAD⁺-Spiegel, sinkt entsprechend die Sirtuin-Aktivität. David Sinclairs Forschungsgruppe an der Harvard Medical School hat diesen Zusammenhang als einen der Schlüsselmechanismen des biologischen Alterns beschrieben.
PARP-Enzyme (Poly-ADP-Ribose-Polymerasen) sind zentral für die Reparatur von DNA-Einzelstrangbrüchen. Auch sie sind strikt NAD⁺-abhängig. Mit zunehmendem Alter häufen sich DNA-Schäden — PARP-Enzyme werden stärker aktiviert und verbrauchen entsprechend mehr NAD⁺. Das Ergebnis ist ein sich selbst verstärkender Kreislauf: mehr Schäden → mehr PARP-Aktivität → weniger NAD⁺ → weniger Sirtuin-Aktivität → weniger Schutz vor weiteren Schäden.
NMN setzt an der Wurzel dieses Kreislaufs an: Es speist den Salvage-Pathway und erhöht die zelluläre NAD⁺-Verfügbarkeit — ohne dabei direkt in Enzymsysteme einzugreifen oder regulatorische Signalwege zu übersteuern.
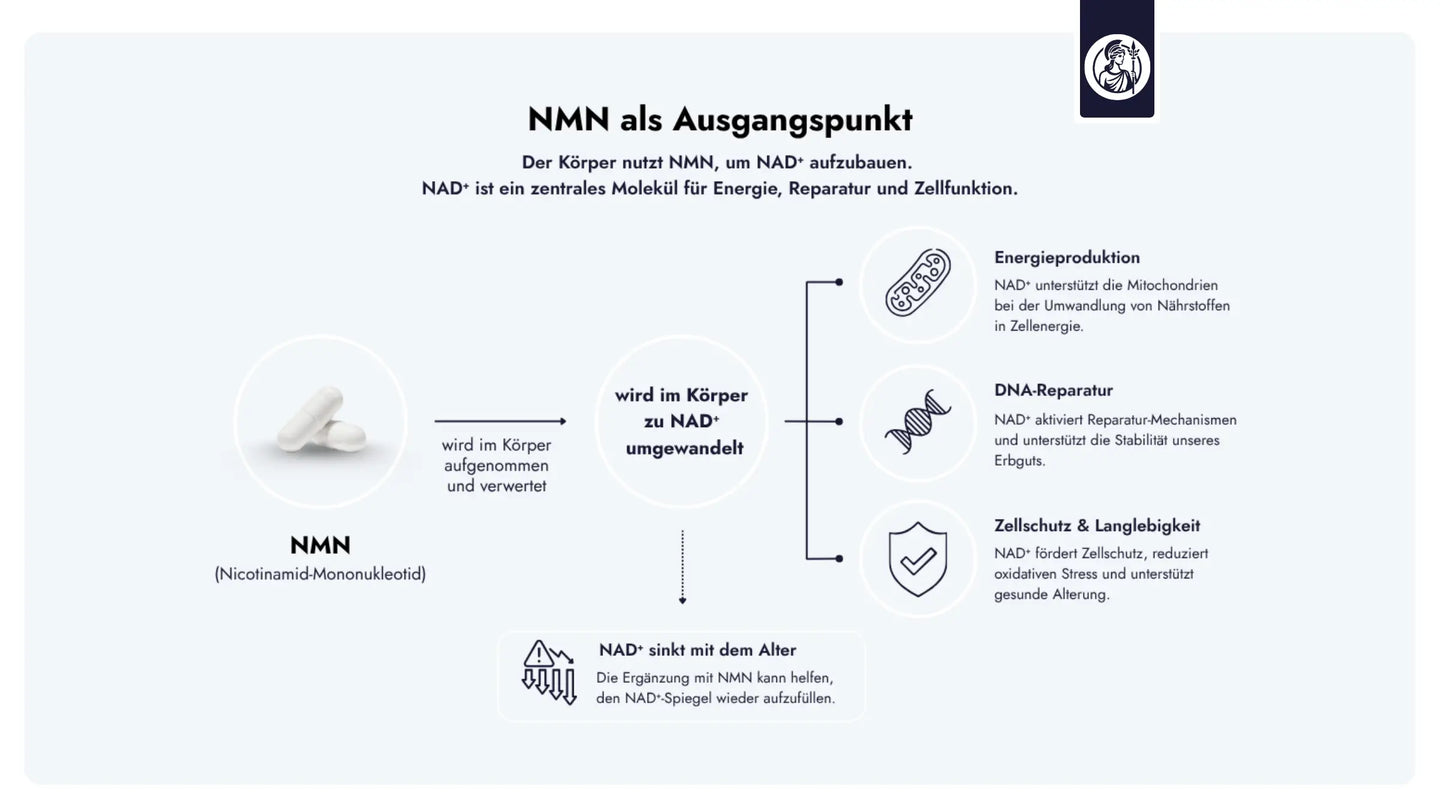
NMN dient als Vorstufe von NAD+ und unterstützt damit zentrale Prozesse wie Energieproduktion, Zellreparatur und Zellschutz.
Die Forschung zu NMN hat in den letzten Jahren erheblich an Umfang gewonnen. Während frühere Studien überwiegend an Nagern durchgeführt wurden, liegen inzwischen mehrere kontrollierte Humanstudien vor, die erste Signale zu Verträglichkeit, Bioverfügbarkeit und Wirkprofil liefern.
Yoshino et al. (2021, Science) untersuchten die Wirkung von oral eingenommenem NMN (250 mg/Tag über 10 Wochen) bei postmenopausalen Frauen mit prädiabetischen Merkmalen. Die Studie zeigte, dass NMN die Insulinsensitivität des Muskelgewebes verbesserte und die Expression von Genen, die mit Muskelremodellierung verbunden sind, positiv beeinflusste — ein Befund, der auf eine metabolische Wirkung hindeutet.
Igarashi et al. (2022, NPJ Aging) dokumentierten in einer placebokontrollierten Studie mit älteren Männern (65+ Jahre), dass 250 mg NMN täglich über 12 Wochen den Blut-NAD⁺-Spiegel signifikant anhob und Ganggeschwindigkeit sowie Griffstärke verbesserte — beides etablierte Marker für muskuloskelettale Gesundheit im Alter. In dieser Studie wurde Uthever® NMN als Prüfsubstanz eingesetzt.
Irie et al. (2020, Endocrine Journal) untersuchten Sicherheit und Verträglichkeit von NMN beim Menschen in einer kontrollierten Einmaldosierungsstudie mit gesunden Erwachsenen. Einzeldosen zwischen 100 und 500 mg wurden ohne unerwünschte Wirkungen toleriert; NAD⁺-Metabolite im Blut stiegen dosisabhängig an. Diese Studie liefert einen der stärksten verfügbaren Belege für die klinische Sicherheit oraler NMN-Gabe beim Menschen.
Die bisherige Humanforschung zu NMN ist vielversprechend, aber noch nicht abgeschlossen. Viele Studien haben kleinere Stichprobengrößen, kurze Studiendauern (8–12 Wochen) und untersuchen spezifische Subpopulationen. Langzeitwirkungen über Jahre sind bisher nicht systematisch untersucht. Für belastbare klinische Aussagen zu Wirksamkeit und Sicherheit fehlen noch größere, multizentrische Phase-III-Studien.
Was die Daten konsistent zeigen: NMN ist beim Menschen gut verträglich, hebt NAD⁺-Marker im Blut messbar an und zeigt in mehreren Studien positive Signale in stoffwechselrelevanten Parametern. NMN ist damit einer der bestuntersuchten Longevity-Wirkstoffe — bei gleichzeitig klarer Notwendigkeit weiterer Forschung.

NMN in Studien: erste Hinweise auf Wirkung und Verträglichkeit.
NMN ist in der Europäischen Union derzeit nicht als Nahrungsergänzungsmittel zugelassen. Es wird offiziell als Forschungsrohstoff (Forschungschemikalie) klassifiziert und darf ausschließlich zu wissenschaftlichen Zwecken vertrieben werden — nicht als Lebensmittel oder Supplement für den allgemeinen Verzehr.
Die rechtliche Grundlage ist die EU Novel Food Regulation (Verordnung (EU) 2015/2283). Diese regelt, welche neuartigen Lebensmittel und Inhaltsstoffe in der EU verkehrsfähig sind. NMN wurde der EU-Kommission zur Prüfung als Novel Food eingereicht — das Verfahren ist laufend. Bis zu einer positiven Entscheidung gilt NMN im EU-Lebensmittelrecht als nicht zugelassener Stoff.
Wichtig: Diese regulatorische Einschränkung sagt nichts über die Sicherheit oder Wirksamkeit von NMN aus. Sie reflektiert den Stand des bürokratischen Zulassungsverfahrens — nicht den wissenschaftlichen Konsens. NMN ist eine körpereigene Substanz, die natürlicherweise im menschlichen Stoffwechsel vorkommt und in Lebensmitteln enthalten ist.
In den USA hat die FDA im September 2025 klargestellt, dass NMN wieder legal als Nahrungsergänzungsmittel vermarktet werden darf — nachdem eine vorübergehende Einschränkung aufgehoben wurde. In Japan, Australien und weiten Teilen Asiens ist NMN bereits seit Jahren als Supplement im Handel erhältlich und wird in zahlreichen klinischen Studien eingesetzt.
Minerva-Vita hält sich vollständig an den geltenden EU-Rechtsrahmen: NMN wird als Forschungsrohstoff deklariert und entsprechend kommuniziert. Diese Transparenz ist kein Disclaimer — sie ist Teil unseres Qualitätsverständnisses.

Die rechtliche Grundlage ist die EU Novel Food Regulation (Verordnung (EU) 2015/2283).
Nicht jedes NMN ist gleich. Die Qualität eines NMN-Rohstoffs hängt von Reinheitsgrad, Herstellungsverfahren, Lagerstabilität und unabhängiger Laborprüfung ab. Minerva-Vita verwendet ausschließlich Uthever® NMN — den weltweit meistzitierten Markenrohstoff in NMN-Humanstudien.
Minerva-Vita verwendet ausschließlich Uthever® NMN und erreicht eine Reinheit von ≥99 % β-NMN — zertifiziert durch unabhängige Drittlabors. Der Rohstoff ist GMP-konform produziert, GRAS-notifiziert (Generally Recognized As Safe, USA) und in mehreren publizierten Humanstudien als Prüfsubstanz eingesetzt worden — darunter die Igarashi-Studie (2022, NPJ Aging). Das ist ein wesentlicher Unterschied zu Commodity-NMN ohne dokumentierte Studienbasis.
NMN ist hygroskopisch — es zieht Luftfeuchtigkeit an und verliert dabei messbar an Stabilität. Kapseln schützen den Wirkstoff vor Oxidation und Feuchtigkeitseintrag, ermöglichen eine exakt reproduzierbare Dosierung und sind geschmacksneutral in der Einnahme. Pulver kann für Anwender mit spezifischen Dosierungspräferenzen sinnvoll sein, erfordert aber konsequente Lagerbedingungen und exaktes Abwiegen.
Minerva-Vita setzt auf HPMC-Kapseln (pflanzlich, vegan) ohne Füllstoffe, Trennmittel oder sonstige Hilfsstoffe. Was in der Kapsel ist: Uthever® NMN. Sonst nichts.

NMN von Minerva-Vita erreicht eine Reinheit von über 99 Prozent.
NMN ist kein isolierter Wirkstoff — es entfaltet seine Wirkung im Kontext des gesamten zellulären Stoffwechsels. Drei Wirkstoffe ergänzen NMN aus biochemischer Sicht besonders sinnvoll: TMG, Ca-AKG und Trans-Resveratrol.
Der Salvage-Pathway, über den NMN in NAD⁺ umgewandelt wird, verbraucht Methylgruppen. Bei intensiver NMN-Supplementierung kann der Bedarf an Methylgruppendonoren ansteigen — mit potenziellen Auswirkungen auf den Homocystein-Stoffwechsel. TMG (Trimethylglycin, auch Betain) wirkt als direkter Methylgruppenspender und stabilisiert diesen Pfad. Die Kombination NMN + TMG ist deshalb in der Longevity-Praxis weit verbreitet und biochemisch gut begründet.
Calcium-Alpha-Ketoglutarat (Ca-AKG) ist ein Zwischenprodukt des Citratzyklus und ein wichtiger Regulator des mTOR-Signalwegs. Es unterstützt die mitochondriale Energieproduktion und spielt eine Rolle bei epigenetischen Regulationsprozessen. In einer 2021 publizierten Humanstudie (Rejuvenation Research, Demidenko et al.) zeigte Ca-AKG-Supplementierung bei älteren Erwachsenen eine messbare Reduktion des biologischen Alters anhand epigenetischer Uhren. Die Kombination mit NMN adressiert komplementäre Stoffwechselwege.
Trans-Resveratrol, ein pflanzliches Polyphenol, gilt als Aktivator von Sirtuin-1 (SIRT1) — einem der NAD⁺-abhängigen Enzyme, die im Kontext von Langlebigkeit am intensivsten erforscht werden. Die Logik der Kombination: NMN erhöht die NAD⁺-Verfügbarkeit als Substrat; Resveratrol aktiviert SIRT1 als Enzym. Ob dieser synergistische Effekt beim Menschen klinisch relevant ist, wird aktuell untersucht — die mechanistische Plausibilität ist gut etabliert (Rajman et al., Cell Metabolism, 2018).
Das Longevity-Trio (NMN + TMG + Ca-AKG) ist der strukturierte Einstieg in einen NMN-basierten Stack — ohne unnötige Komplexität, mit klarer biochemischer Begründung für jede Komponente.

Das Longevity-Trio kombiniert NMN, CaAKG und Betain (TMG) - 3 Wirkstoffe aus der Longevity-Forschung.
NMN ist in der Europäischen Union derzeit nicht als Nahrungsergänzungsmittel zugelassen. Es wird offiziell als Forschungsrohstoff deklariert und darf ausschließlich zu wissenschaftlichen Zwecken vertrieben werden. Die EU-Kommission prüft NMN im Rahmen der Novel Food Regulation (Verordnung (EU) 2015/2283). Außerhalb der EU — insbesondere in den USA und Asien — ist NMN bereits weit verbreitet und wurde in zahlreichen Studien am Menschen untersucht.
NMN und NR (Nicotinamid-Ribosid) sind beides NAD⁺-Vorstufen. Der strukturelle Unterschied liegt in der Phosphatgruppe, die NMN zusätzlich trägt. NR muss im Körper erst in NMN umgewandelt werden, bevor es als NAD⁺ verfügbar ist — NMN tritt diesen Schritt direkt an und liegt damit eine Stufe näher an NAD⁺.
In wissenschaftlichen Studien wird NMN meist morgens auf nüchternen Magen eingenommen. NAD⁺ ist eng mit dem zirkadianen Rhythmus verknüpft — NAD⁺-abhängige Enzyme wie Sirtuine spielen nicht nur bei der DNA-Reparatur, sondern auch bei der Regulation der inneren Uhr eine Rolle. Eine morgendliche Einnahme unterstützt die natürliche Phasenlage des NAD⁺-Metabolismus.
Die Synthese von NAD⁺ aus NMN über den Salvage-Pathway verbraucht Methylgruppen. TMG (Trimethylglycin) wirkt als Methylgruppenspender und unterstützt den Homocystein-Stoffwechsel. Die Kombination von NMN und TMG ist deshalb aus biochemischer Sicht sinnvoll — TMG kompensiert den erhöhten Methylgruppenbedarf im NAD⁺-Syntheseweg.
NMN ist ein hygroskopisches Molekül — es zieht Feuchtigkeit an und verliert dabei an Stabilität. Kapseln schützen den Wirkstoff vor Oxidation und Feuchtigkeit, ermöglichen eine präzise Dosierung und sind geschmacksneutral. Pulver bietet Flexibilität in der Dosierung, erfordert jedoch exakten Umgang und ist empfindlicher gegenüber Lagerungsbedingungen.
NMN wird primär von Personen untersucht, die ihren NAD⁺-Haushalt im Rahmen einer gezielten Longevity-Strategie unterstützen möchten. Da NMN in der EU als Forschungsrohstoff klassifiziert ist, empfehlen wir, die Einnahme vorab mit einer Ärztin oder einem Arzt zu besprechen — insbesondere bei bestehenden Erkrankungen oder Medikamenteneinnahme.
Yoshino M. et al. (2021). Nicotinamide mononucleotide increases muscle insulin sensitivity in prediabetic women. Science, 372(6547), 1224–1229. doi.org/10.1126/science.abe9985
Igarashi M. et al. (2022). Chronic nicotinamide mononucleotide supplementation elevates blood nicotinamide adenine dinucleotide levels in healthy older men. NPJ Aging, 8(1), 5. doi.org/10.1038/s41514-022-00084-z
Irie J. et al. (2020). Effect of oral administration of nicotinamide mononucleotide on clinical parameters and nicotinamide metabolite levels in healthy Japanese men. Endocrine Journal, 67(2), 153–160. doi.org/10.1507/endocrj.EJ19-0313
Grozio A. et al. (2019). Slc12a8 is a nicotinamide mononucleotide transporter. Nature Metabolism, 1(1), 47–57. doi.org/10.1038/s42255-018-0009-4
Rajman L., Chwalek K. & Sinclair D.A. (2018). Therapeutic potential of NAD-boosting molecules: the in vivo evidence. Cell Metabolism, 27(3), 529–547. doi.org/10.1016/j.cmet.2018.02.011
Uthever® NMN von Minerva-Vita
 NMN Kapseln (Uthever®) | 500 mg
500 mg Uthever® NMN · 60 Kapseln
€44,90
Zum Produkt →
NMN Kapseln (Uthever®) | 500 mg
500 mg Uthever® NMN · 60 Kapseln
€44,90
Zum Produkt →
 NMN 90-Tage-Kur: NAD+ Support
3-Monats-Bundle · Mengenrabatt
€119,70
Zum Produkt →
NMN 90-Tage-Kur: NAD+ Support
3-Monats-Bundle · Mengenrabatt
€119,70
Zum Produkt →
 Longevity-Trio: NMN, Ca-AKG & TMG
NMN + TMG + Ca-AKG · Longevity-Trio
€99,70
Zum Produkt →
Longevity-Trio: NMN, Ca-AKG & TMG
NMN + TMG + Ca-AKG · Longevity-Trio
€99,70
Zum Produkt →
Weiterführende Artikel
* NMN (β-Nicotinamid-Mononukleotid) ist in der Europäischen Union derzeit nicht als Nahrungsergänzungsmittel zugelassen. Das Produkt wird als Forschungsrohstoff angeboten und ist nicht für den Verzehr bestimmt. Nahrungsergänzungsmittel sind kein Ersatz für eine ausgewogene Ernährung. Die empfohlene Tagesdosis darf nicht überschritten werden. Außerhalb der Reichweite von Kindern aufbewahren.
